Galvanische Zellen 1 Einführung . Galvanische Zelle und Elektrolyse
Автор: Thomas Zimmer
Загружено: 2026-01-09
Просмотров: 18
Описание:
Hier der Link zum Skript: https://td2ec2in2euwest.teamdrive.net...
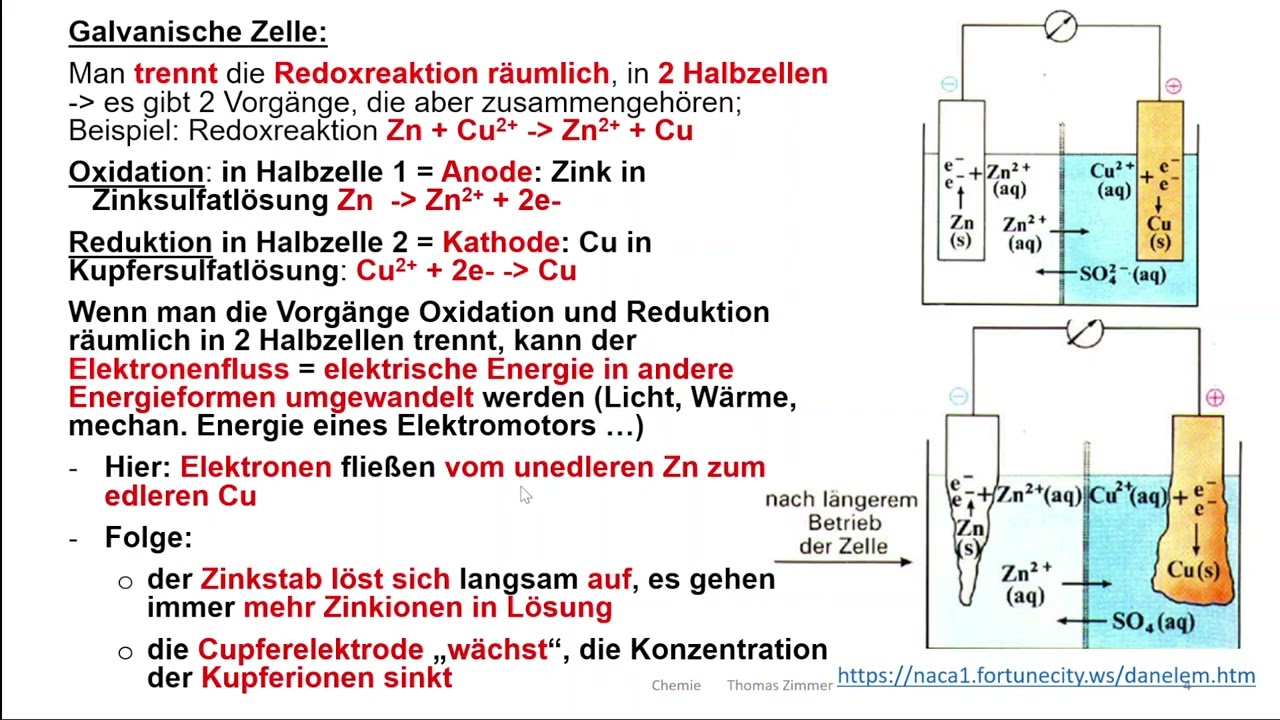
Galvanische Zelle: Umwandlung chem. E in elektr. E (Batterie, Akku); die chem. Reaktion läuft von allein
Elektrolyse: Umwandlung elektr. E in chem. E; die Reaktion läuft nicht von allein, sondern benötigt die Zufuhr von (elektrischer) Energie
Elektrochemische Reaktion findet an Elektroden statt, die in einer Elektrolytlösung sind.
Die Polarität (Plus- oder Minuspol) hängt von der Art der Zelle ab
In einer galvanischen Zelle (Stromerzeugung) ist die Anode der Minuspol (negative Ladung, Oxidation) und die Kathode der Pluspol (positive Ladung, Reduktion).
Bei einer elektrolytischen Zelle (Stromeinspeisung / Stromverbrauch) ist die Anode der Pluspol und die Kathode der Minuspol
Повторяем попытку...
Доступные форматы для скачивания:
Скачать видео
-
Информация по загрузке:



















