Молекулярная орбитальная диаграмма многоатомных молекул CO2 – Химические связи и молекулярные стр...
Автор: Edmerls
Загружено: 2020-10-23
Просмотров: 98154
Описание:
Молекула диоксида углерода (CO2) трёхатомна и линейна, как и дигидрид бериллия (BeH2). Однако, в отличие от водорода, который является периферийным атомом в BeH2, в CO2 есть атомы кислорода, которые имеют p-орбитали. Следовательно, в молекуле CO2 больше молекулярных орбиталей, чем в молекуле BeH2. Электронная конфигурация атомов C и O:
C (6) 1s2 2s2 2p2
O (8) 1s2 2s2 2p4
В молекуле CO2 углерод является центральным атомом, а два атома кислорода — периферийными. Таким образом, сначала орбитали периферийных атомов, т.е. атомов кислорода, перекрываются, образуя групповые орбитали, а затем эти групповые орбитали перекрываются с атомными орбиталями атома углерода. Теперь мы рассмотрим формы групповых орбиталей и попытаемся одновременно сопоставить их с формой атомных орбиталей атома углерода.
Во-первых, 2s-орбитали атомов кислорода не участвуют в связывании. Итак, возьмем 2pz-орбитали первого и второго атомов кислорода, выровненные по направлению оси перекрытия. Таким образом, их можно объединить с одинаковыми знаками на каждой доле, чтобы сформировать групповую орбиталь пси 1. Если мы попытаемся вставить атом углерода между двумя атомами кислорода, центральный лепесток групповой орбитали может легко перекрыться с 2s-орбиталью атома углерода. Этот тип перекрытия приведет к образованию сигма-s-орбиталей и сигма-звезды s-орбиталей, если знаки этих орбиталей противоположны. Если знаки 2pz-орбиталей кислорода различны, то происходит вычитание и образуется пси-орбиталь группы пси 2, имеющая симметрию, совпадающую с 2pz-орбиталью атома углерода. Таким образом, они дадут две сигма-связи, такие как сигма-z и сигма-звезда z, в зависимости от знака долей. Аналогично, 2px-орбитали кислорода объединяются, чтобы дать пси-орбиталь группы пси 3, которая имеет симметрию, совпадающую с 2px-орбиталью атома углерода. Итак, это также приведет к образованию двух связей, но в этом случае, поскольку перекрывающиеся доли находятся в перпендикулярном положении оси перекрытия, вместо сигма-связи образуется пи-связь. Их можно обозначить как молекулярные орбитали pi z и pi star z. В случае, если знаки долей 2px-орбиталей кислорода различны, происходит вычитание для формирования групповой орбитали pi 4. Как вы можете видеть, эта групповая орбиталь имеет положительный и отрицательный заряд на чередующихся концах, поэтому в атоме углерода нет соответствующей орбитали. Таким образом, эта групповая орбиталь остается несвязывающей молекулярной орбиталью. Подобно px-орбитали, существует py-орбиталь под углом 90 градусов к направлению x и z, поэтому они также объединяются, чтобы дать групповую орбиталь psi 5, и эта групповая орбиталь совпадает с 2py-орбиталью атома углерода. Таким образом, это также создаст пи-связь, поскольку перекрытие перпендикулярно оси связи. Если знаки долей противоположны, то происходит вычитание, образуя групповую орбиталь пси 6, которая не имеет соответствующей симметрии с атомными орбиталями углерода и остаётся несвязывающей молекулярной орбиталью.
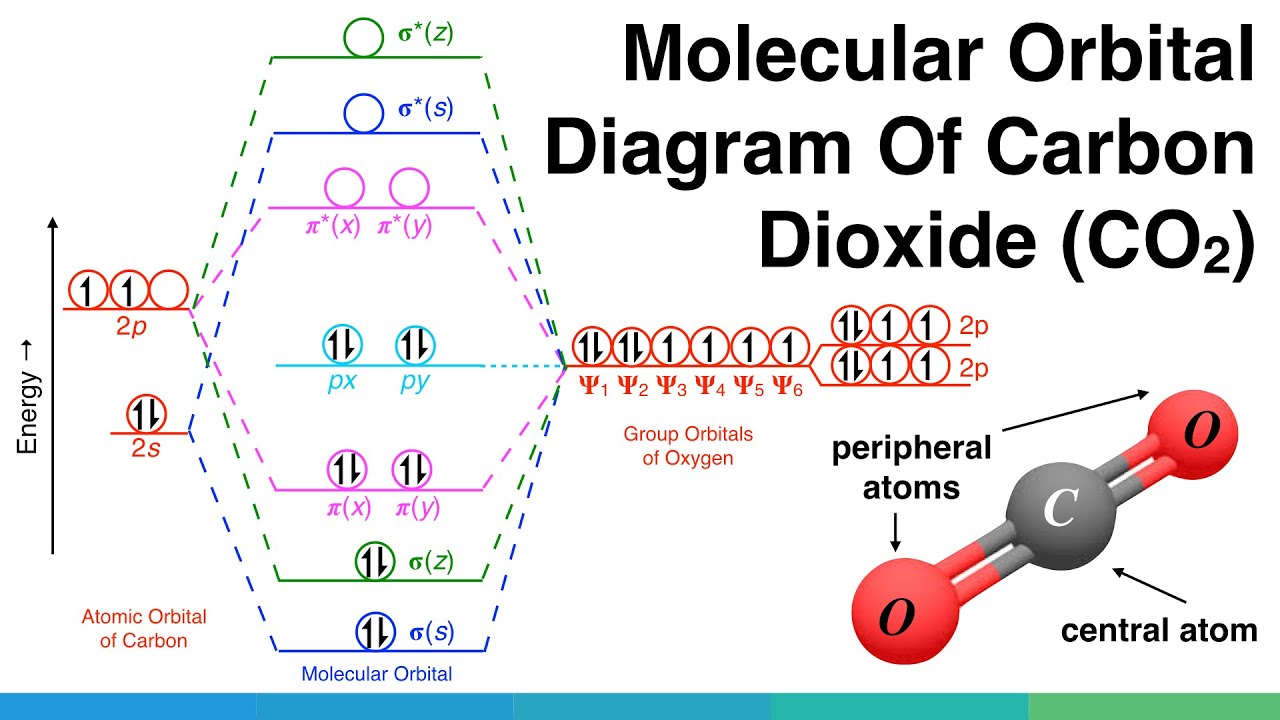
Теперь попробуем изобразить все эти орбитали в виде диаграммы молекулярных орбиталей. Справа мы снова изобразили атомные орбитали атомов кислорода, которые при их объединении образуют групповую орбиталь 6. Эти групповые орбитали будут перекрываться с атомными орбиталями углерода, показанными слева.
Итак, во-первых, пси 1 перекрывается с 2s-орбиталью, образуя молекулярные орбитали sign s и sigma star s. Во-вторых, пси 2 перекрывается с 2pz-орбиталями углерода, поскольку это аксиальное перекрытие, образующаяся связь будет сигма-связью, а именно сигма-z и сигма-star z. Затем пси-3 и пси-5 перекрываются с px- и py-орбиталями, поскольку обе орбитали перпендикулярны оси z, перекрытие происходит латерально к ней, образуя π-связи. Таким образом, образуются связывающие π-x и π-y орбитали, а также разрыхляющие π-звезда x и π-звезда y молекулярные орбитали.
И наконец, π-4 и π-6 остаются несвязывающими, поскольку в атоме углерода отсутствует соответствующая симметрия.
Теперь на этих молекулярных орбиталях из молекулярных орбиталей с самой низкой энергией могут разместиться 12 электронов: четыре электрона углерода и восемь электронов двух атомов кислорода.
Следовательно, из диаграммы молекулярных орбиталей электронная конфигурация молекулы CO2 может быть представлена как (αs)₂, (αz)₂, (αx)₂, (αy)₂.
Поскольку на молекулярных орбиталях нет неспаренных электронов, CO2 является диамагнитной молекулой.
Другие предметы:
Образование для взрослых @ http://www.edmerls.com/index.php/Adul...
Аналитическая химия @ http://www.edmerls.com/index.php/Anal...
Прикладная физика @ http://www.edmerls.com/index.php/Appl...
Инженерное черчение @ http://www.edmerls.com/index.php/Engi...
Английский язык @ http://www.edmerls.com/index.php/Engl...
Экология @ http://www.edmerls.com/index.php/Envi...
Общая медицина @ http://www.edmerls.com/index.php/Gene...
Математика @ http://www.edmerls.com/index.php/Math...
Органическая ...
Повторяем попытку...
Доступные форматы для скачивания:
Скачать видео
-
Информация по загрузке:






![Пожалуй, главное заблуждение об электричестве [Veritasium]](https://imager.clipsaver.ru/6Hv2GLtnf2c/max.jpg)




![Как представить 10 измерений? [3Blue1Brown]](https://imager.clipsaver.ru/tCIARwH01Ac/max.jpg)